Publié le 21 sep 2022Lecture 5 min
Mélanome malin : l’échappement aux immunothérapies, la problématique centrale de l’oncologie de précision
Hélène JOUBERT, Paris - D’après la « Keynote Lecture Future therapies in malignant melanoma » du Pr Olivier Michielin, 18e congrès de l’European association of dermatology oncology (EADO), Séville, 21-23 avril 2022
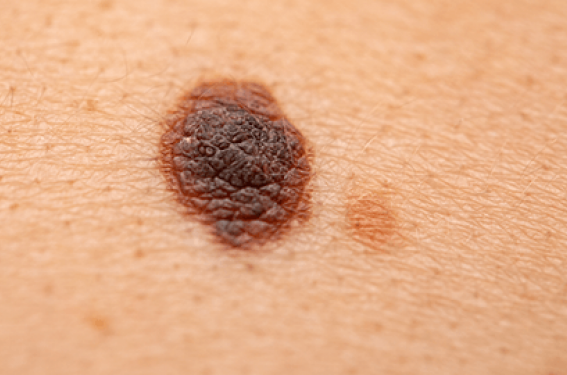
Alors que les immunothérapies, principalement les anti-PD1, règnent en maîtres dans le traitement du mélanome malin – dans la situation métastatique mais également adjuvante allant jusqu’à parler de guérison chez certains patients – les recherches en oncologie de précision portent aujourd’hui sur les phénomènes d’échappement et les gains incrémentaux de ces stratégies en termes de survie.
La problématique actuelle dans le mélanome malin est en ligne directe avec les progrès obtenus jusqu’à très récemment. En passant en une décennie d’une pathologie au pronostic très sombre à une rémission sur le long terme (six ans environ)(1) pour un peu plus de 50 % de patients, et où le terme de guérison peut être employé du fait d’un risque de décès rejoignant celui de la population saine(2), « le moteur des recherches actuelles est de comprendre pourquoi une thérapie jusque-là performante est mise en échec chez une fraction importante de patients, résume le Pr Olivier Michielin, médecin chef du Centre d’oncologie de précision et responsable de la Consultation spécialisée du mélanome (département d’oncologie UNIL, centre hospitalier universitaire vaudois, CHUV de Lausanne). Il nous faut distinguer les mécanismes spécifiques, que l’échappement soit inné ou acquis après une période de relative efficacité. Les facteurs prédictifs d’échappement commencent à être identifiés (perte du CMH de classe I par la tumeur, altérations de la voie IFN-gamma…), mais la complexité des mécanismes souvent intriqués est extrême, impliquant la tumeur elle- même, l’épuisement du système immunitaire ou encore le recrutement de cellules myéloïdes immunosuppressives. »
Les immunothérapies ainsi que les thérapies ciblées obtiennent des résultats spectaculaires dans le mélanome (dans les situations métastatique et adjuvante), même si le bénéfice sur le long terme des immunothérapies semble plus important(3), les positionnant comme pièce centrale de l’arsenal thérapeutique contre le mélanome malin. Ces thérapeutiques ont révolutionné le traitement du mélanome, en particulier les anticorps monoclonaux inhibiteurs de checkpoints immunitaires anti-PD-1. Ils ciblent des récepteurs de surface inhibiteurs des lymphocytes (CTLA-4 ou PD-1), réactivant ainsi une réponse immunitaire antitumorale souvent activement inhibée par les cellules tumorales. Pour sa part, la chimiothérapie ne conserve qu’une place marginale (bridges, etc.) dans l’algorithme thérapeutique.
Thérapies futures et multithérapies en cas d'échec
Lorsque les résultats avec les anti-PD1 sont insuffisants, laissant la maladie progresser, les travaux portent alors sur les combinaisons de molécules. Les études concluantes sur la combinaison anti-PD1/anti-LAG3 en comparaison avec l’anti-PD1 seul sont un exemple de progrès récent en termes de gains incrémentaux. En attendant une com paraison directe ou une triple association, la combinaison anti-CTLA-4 et anti-PD-1 reste aujourd’hui l’une des options les plus performantes dans le mélanome métastatique ou inopérable, notamment en cas de métastases cérébrales, et ceci en dépit d’une forte toxicité. « Il nous faut désormais déterminer “la bonne molécule ou combinaison de molécules délivrée(s) au bon moment”, poursuit le Pr Olivier Michielin. Au-delà des tests génomiques, l’oncologie de précision interroge le système immunitaire (le type de lymphocytes et d’autres cellules immunitaires infiltrant la tumeur, la biologie sous-jacente), la biologie de la tumeur elle- même et les caractéristiques cliniques du patient (les sites de métastatisation, l’historique des traitements ou la cinétique de la maladie), afin de définir la stratégie optimale (schéma d’ad ministration, nature de la combinaison, séquences thérapeutiques, etc.). En sus, la transcriptomique au niveau cellulaire ou séquençage des ARNm sur cellules uniques (Single Cell RNA Seq) se focalise sur l’homéostasie cellulaire au sein de la tumeur, qui renseigne sur les mécanismes d’échappement immunitaire. »
40 cibles potentiellement intéressantes
D’anciennes cibles sont en train d’être reconsidérées, comme les anticorps anti-CTLA-4 (ipilimumab) qui font place à de nouvelles générations d’anticorps monoclonaux. Certains possèdent la propriété de permettre la déplétion de certains types de cellules, dont les lymphocytes T régulateurs au rôle inhibiteur (par exemple l’ipilimumab-NF qui déplète les T régulateurs). Parmi les nouvelles cibles, la prometteuse LAG3 (pour « Lymphocyte-activation gene 3 ») ou CD223 est une protéine jouant un rôle d’inhibiteur de point de contrôle, molécule de surface cellulaire exprimée sur les lymphocytes T activés et en état d’épuisement immun(4). Une kyrielle de nouvelles thérapies, dont les antiangiogéniques, font l’objet de recherches. À ce propos, l’inhibiteur multikinase lenvatinib a démontré un intérêt en deuxième ligne après échappement aux immunothérapies (mélanomes de stades IV après échec d’anti-PD-1). Les anti-IL8 (anti-interleukine 8) ont pour leur part un rôle à jouer pour prévenir le recrutement de neutrophiles immunosuppresseurs au sein de la tumeur. L’ingénierie moléculaire a aussi permis un progrès considérable dans le mélanome oculaire avec le tebentafusp(5). Cette protéine bispécifique est constituée d’un récepteur antigénique à affinité renforcée pour un peptide dérivé de la glycoprotéine 100 présenté par HLA-A2. Il est fusionné à un activateur CD3 qui permet de stimuler les lymphocytes T de voisinage. Cette double fonctionnalité (cibler de manière spécifique les tumeurs et activer en même temps le système immunitaire local) est un mécanisme général potentiellement intéressant dans le traitement du mélanome mais également dans d’autres types de cancers. Le tebentafusp est en cours d’approbation dans le mélanome oculaire.
En parallèle, d’autres chemins d’activation sont explorés, dont la voie essentielle cGAS-STING. Il s’agit d’un composant du système immunitaire inné destiné à détecter la présence d’ADN bicaténaire dans le cytosol des cellules d’eucaryotes et à déclencher en réponse l’expression de gènes inflammatoires pouvant conduire à l’activation de mécanismes de défense. Si des molécules stimulant la voie cGAS-STING sont extrêmement intéressantes, leur développement n’est encore qu’à un stade préliminaire. « Globalement, la re cherche dans le mélanome malin bénéficie d’un dynamisme exceptionnel, avec des résultats publiés en continu, chaque mois, salue le Pr Olivier Michielin. Ceci grâce à un tissu de recherche translationnelle consistant et très organisé. C’est pourquoi le mélanome reste l’une des maladies phares dans le développement des immunothérapies. »
Publié dans Dermatologie Pratique
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


